Herstellung von Kunststoffen
Sonstige Polymerisationsreaktionen
Auf dieser Seite sollen der Vollständigkeit halber noch kurz einige weitere Arten von Polymerisationsreaktionen vorgestellt werden:
Ziegler-Natta-Polymerisation
Die Ziegler-Natta-Polymerisation wurde von zwei Chemikern entwickelt, Karl Ziegler und Giulio Natta (wer hätte das gedacht?), die 1963 gemeinsam den Nobelpreis für Chemie erhielten.
Sie dient zur Herstellung von Polymeren mit bestimmter Taktizität, insbesondere zur Herstellung von isotaktischem Polypropen, und außerdem zur Herstellung von linearem Polyethen (bei der radikalischen Polymerisation von Ethen entsteht aufgrund von Kettenübertragungsreaktionen verzweigtes Polyethen).
Doch wie funktioniert es?
Für die Reaktion werden bestimmte Katalysatoren (Ziegler-Natta-Katalysatoren) verwendet, die Komplexe mit den reagierenden Teilchen ausbilden und die Monomere und die wachsenden Molekülketten so festhalten, dass sie nur in einer bestimmten Weise reagieren können. Der Mechanismus für diese Reaktion ist so kompliziert, dass er noch nicht endgültig geklärt ist, aber auf jeden Fall funktioniert es, und das ist schließlich die Hauptsache (zumindest in der Kunststoffindustrie).
Ziegler-Natta-Katalysatoren
Ein solcher Katalysator besteht aus zwei Komponenten, dem eigentlichen Katalysator und einem Co-Katalysator, die zusammen einen Komplex bilden, an den sich Monomere anlagern können. Bei dem Katalysator handelt es sich um Übergangsmetallverbindungen, meist von Titan und Vanadium (die Übergangsmetalle werden auch Nebengruppenelemente genannt, sie stehen in der Mitte des Periodensystems), der Co-Katalysator ist normalerweise eine Aluminium-organische Verbindung, d.h. eine Verbindung, bei dem an ein Aluminiumatom organische Reste gebunden sind. Zwei typische Katalysatorsysteme sind folgende:
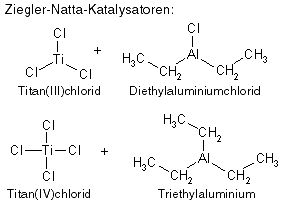
Titan kann insgesamt 6 Komplexliganden binden, und zunächst bildet sich ein Komplex aus Katalysator und Co-Katalysator, bei dem allerdings noch eine Bindungsstelle frei bleibt: Hier kann sich ein Monomer anlagern (für das andere Katalysatorsystem funktioniert die Komplexbildung nach demselben Prinzip).
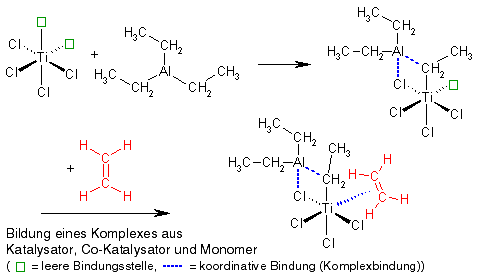
Wachstumsreaktion
Das Kettenwachstum geschieht durch eine sogenannte "Einschiebungsreaktion": Das Monomere, das als Ligand an das Titaniumatom gebunden ist, schiebt sich zwischen das Titaniumatom und das Kohlenstoffatom, das ebenfalls an das Titaniumatom gebunden ist. Im Komplex gibt es nun wieder eine freie Bindungsstelle, an die sich ein anderes Monomer anlagern kann, das sich ebenfalls zwischen die wachsende Molekülkette und das Titaniumatom schiebt usw.
In der folgenden Zeichnung ist nur die erste Einschiebungsreaktion gezeigt, und der Co-Katalysator mit Aluminiumatom usw. ist nicht dargestellt, um das Ganze etwas übersichtlicher zu machen.
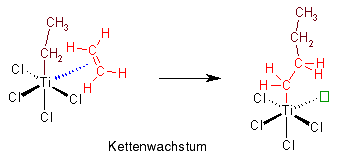
Doch wie bekommt man Kunststoffe mit unterschiedlicher Taktizität?
Durch die Wahl des Katalysatorsystems kann man die Taktizität eines Kunststoffes festlegen. Für die Herstellung von isotaktischem Polypropen z.B. verwendet man das System TiCl3 und Al(C2H5)2Cl (s.o.), syndiotaktisches Polypropen hingegen erhält man, wenn man als Katalysatorsystem VCl4 und Al(C2H5)2Cl verwendet, also Titan durch Vanadium, ein anderes Übergangsmetall, ersetzt, denn dann werden die Monomere bei der Einschiebungsreaktion so gedreht, dass die Methylgruppen an der Kette am Ende abwechselnd nach links und nach rechts zeigen.
Ringöffnungspolymerisation
Bei der Ringöffnungspolymerisation reagieren cyclische Monomere, d.h. Monomere, die aus Ringen bestehen, zu linearen Molekülketten. Doch wie funktioniert das?
Natürlich müssen die Ringe aufgehen, um zu Molekülketten werden zu können, wofür normalerweise ein Initiator benötigt wird. Wenn die Ringöffnungspolymerisation z.B. als Kationische Polymerisation abläuft, handelt es sich bei dem Initiator also um eine ![]() Lewis-Säure. Die Reaktion funktioniert nicht mit allen beliebigen cyclischen Molekülen, sondern nur mit solchen, die bereits eine Art Schnittstelle haben, an der sie sich öffnen können. Und eine noch wichtigere Voraussetzung ist, dass beim Öffnen des Rings zwei funktionelle Gruppen entstehen (hier dargestellt als A und B), an denen die geöffneten Ringe miteinander reagieren können, sodass ein Polymer entsteht.
Lewis-Säure. Die Reaktion funktioniert nicht mit allen beliebigen cyclischen Molekülen, sondern nur mit solchen, die bereits eine Art Schnittstelle haben, an der sie sich öffnen können. Und eine noch wichtigere Voraussetzung ist, dass beim Öffnen des Rings zwei funktionelle Gruppen entstehen (hier dargestellt als A und B), an denen die geöffneten Ringe miteinander reagieren können, sodass ein Polymer entsteht.
Das Ganze kann man sich schematisch folgendermaßen vorstellen:
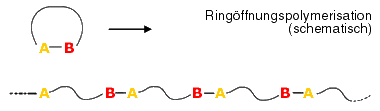
Die Ringöffnungspolymerisation ist nicht immer eine wirkliche ![]() Polymerisation, denn sie kann auch als
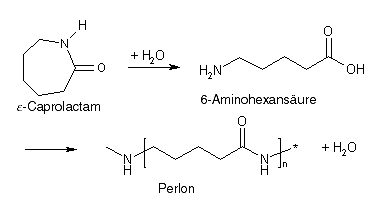
Polymerisation, denn sie kann auch als ![]() Polykondensation in Stufen verlaufen, wie das wohl berühmteste Beispiel einer Ringöffnungspolymerisation, die Herstellung von Perlon aus ε-Caprolactam, zeigt.
Polykondensation in Stufen verlaufen, wie das wohl berühmteste Beispiel einer Ringöffnungspolymerisation, die Herstellung von Perlon aus ε-Caprolactam, zeigt.
Copyright © mk 2000