Eine Untersuchung zur Anwendung des Ge-Se-Resistsystems für die Mikrolithographie thomas1 zeigt, daß bei einer Zusammensetzung des Resists von Ge0.2Se0.8 die Empfindlichkeit gegenüber Quecksilberdampflampenlicht maximal ist. Hierbei ist die Empfindlichkeit mehr als 30 mal größer als die der Verbindung GeSe2. Aufgrund der chemisch-physikalischen Ähnlichkeit von Germaniumselenid und Germaniumsulfid liegt es nahe, das Analoge für GeSx anzunehmen. Für die hochauflösende Mikrolithographie sind stabile amorphe, nichtkristalline Schichten notwendig. Die Tendenz zu amorphen GeSx-Verbindungen steigt mit höherem x kawamoto1,kawamoto2. Damit liegt die Verwendung von GeSx mit x > 2 nahe. Dies Ausgangsmaterial ist im Handel nicht erhältlich. Nur die stöchiometrischen Verbindungen GeS und GeS2 sind über den Versandhandel aus den USA zu beziehen. Für die Erzielung der optimalen Zusammensetzung des Resists bedeutet dies, daß das Ausgangsmaterial selbst hergestellt werden muß.
GeSx mit x > 2 läßt sich auf chemischen Reaktionswegen nicht gewinnen, da solche Verbindungen nicht der Stöchiometrie entsprechen. Ein Verfahren zur Herstellung von GeSx mit x > 2 ist die Herstellung der massiven Verbindung im Schmelzofen.
Ählich wie in einer Arbeit von Tanaka tanaka1
wurden Legierungen von Germanium mit Schwefel hergestellt.
Germanium und Schwefel wurden im
gewünschten Atomzahlenverhältnis (siehe Tabelle)
gemischt, pulverisiert und in einseitig verschlossene Quarzrohre
gefüllt. Germanium und Schwefel waren sehr rein bei einem
Reinheitsgrad von 99.999 %.
X-Wert Gewichtsanteil Ge Gewichtsanteil S Gewichtsverhältnis S/Ge 2 0.53 0.47 0.88 3 0.43 0.57 1.33 3.5 0.39 0.61 1.55
Mittels einer Wasserstrahlpumpe wurden
die Rohre evakuiert, wobei der Restdruck im Rohr ca. 25 hPa
betragen hat. Das Quarzrohr wurde dann mit einem
Azethylen-Sauerstoff-Schweißbrenner zugeschmolzen. Um die
Spannungen bei der Abkühlung an der Schmelzstelle zu verringern,
wurde diese langsam abgekühlt. Die Quarzrohre
hatten einen Außendurchmesser von 6 mm und eine Wandtärke von
1 mm. Diese sollten laut eines technischen Datenblattes gti einem Innendruck von gut
25 atü standhalten. Quarzrohre von größerem Durchmesser ließen
sich nicht mehr sauber zuschmelzen. Der Schmelzofen
besteht aus einer leichten keramischen Isolationsmasse, in die die
elektrisch betriebene Heizwendel eingebettet ist. Dieses Ofenelement
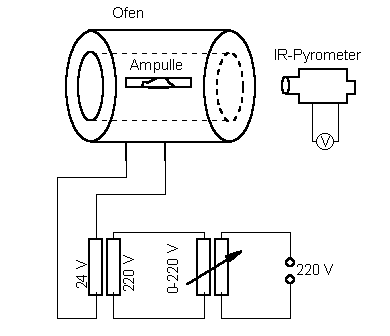
wurde von der Fa. Fibrothal Walddorf-Mörfelden bezogen. Mittels zweier Transformatoren wurde der
Ofen angesteuert (siehe Abb. ). Die Temperaturmessung
erfolgte über ein Pyrometer [Fa. Heimann] durch eine Öffnung im
Ofen. Das Pyrometer erfaßt die IR-Strahlung quantitativ und gibt
eine Spannung aus, die proportional zur Temperatur ist.

Aufbau zu den Legierversuchen
Die gefüllten Quarzampullen wurden in den Ofen gelegt und innerhalb von 3 Stunden auf 800oC aufgeheizt. Nach einem Tag wurde die Temperatur auf 970-1000oC erhöht und für mindestens 3 Tage konstant gehalten. Innerhalb dieser Zeit wurden die Ampullen einige Male leicht geschwenkt, um die Durchmischung der Schmelze zu begünstigen. Schließlich wurden die Ampullen an der Luft abgekühlt und mit einer Zange aufgebrochen. Das Legiergut wurde von den Quarzsplittern durch Verlesen getrennt und in Schnappdeckelgläsern verwahrt. Die x=2-Verbindung war augenscheinlich homogen und zeigte eine bräunliche Transparenz. Die x=3 und 3.5-Verbindung erschien grau gesintert. Germanium schmilzt unter Normaldruck bei 958.5oC tabchem, so daß diese Temperatur erreicht werden muß, um eine Durchmischung von Germanium und Schwefel zu erzielen. Schwefel entwickelt bei Temperaturen von 970oC einen Dampfdruck von 6.5 atü l-b. Die Dichte von Germanium beträgt 5.35 g/cm3, die des Schwefels 1.92 g/cm3 (amorphe Modifikation bei Normalbedingungen). Dieser Dichteunterschied wirkt einer Durchmischung entgegen. Eine mechanische Stimulierung der Durchmischung ist schwierig, da die heißen Ampullen schwer zu handhaben sind. Wahrscheinlich aufgrund von unperfekten Abschmelzungen kam es ab und an zum Bersten von Ampullen. Die Quarzampullen werden daher im Ofen in Keramikrohren gelagert, um bei einem möglichen Bersten der Ampullen eine Beschädigung der Ofeninnenwände zu verhindern. In jede Ampulle wurde etwa 2 g Material eingefüllt und nach dem Legieren für die folgenden Untersuchungen verwandt. Wie sich später herausstellte waren diese Legierungen inhomogen, d.h. Reste von Schwefel oder stark schwefelhaltige Anteile waren mit stark germaniumhaltigen Anteilen vermischt. Bei der nachfolgenden Vakuumverdampfung kam es so zur starken Disproportionierung (siehe Abb. ).
Die während meiner Diplomarbeit in einer Vakuumapparatur aufgedampften Schichten zeigten starke Inhomogenitäten xx. Die Schichten waren nach der Entwicklung von vielen großen Löchern übersäht. Aufgrund der Vielzahl möglicher Parameter konnte die Ursache nicht festgestellt werden. Der Druck in der Vakuumapparatur betrug bestenfalls 10-2 Pa. Das Restgas war mit Kohlenwasserstoffverbindungen aus der Diffusionspumpe bzw. der Rotationspumpe versetzt. Des weiteren war das Legiergut nicht optimal. Außerdem neigt Germaniumsulfid bei starker Erhitzung zur Disproportionierung.
In einem Artikel von Chen und Lauks wird von der Löslichkeit
von GeSe in organischen Lösungsmitteln wie Diäthylamin, Triäthylamin und
Propylamin berichtet. Die Autoren nutzen dies, um dünne Schichten
aufzuschleudern.
Viele organische Lösungsmittel lösen Metalle oder Metallverbindungen in Komplexen.
Durch Ausdampfen des Löungsmittels können die Metalle bzw. Metallverbindungen
wieder freigesetzt werden. Organische Verbindungen, die die zu komplexierende
Atomgruppe mit aktiven Molekülteilen in die Zange nehmen, werden in der Chemie
Chelate(griechisch: chele = Krebsschere) genannt mortimer.
Am Äthylendiamin, einem klassischen Vertreter der Chelate, läßt sich die
komplexe Ringbildung durch Chelatierung zeigen (siehe Abb. ). Mit den in
Tabelle (|x bzw. x markieren die freien
Elektronenpaare, über die die Bindung erfolgt)
aufgeführten
organometallischen Komplexbildnern wurden Lösungsversuche mit
GeSx (x=2 bzw. 3) unternommen.
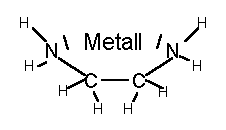
Chelatierung mit Äthylendiamin
Lösungsmittel Konzentration Formel Äthandiol 99% H-O-CH2-CH2-O-H Äthandiol 30% in Wasser |O-CH-CH-O| Diäthylamin 99% CH3-CH2-N-CH2-CH3 Äthylendiamin 99% NH2-CH2-CH2-NH2
Von diesen bilden die beiden Amine über die freien Elektronenpaare am Stickstoff und die anderen
über die freien Elektronenpaare am Sauerstoff Bindungen zum Metall
aus. Nur Äthylendiamin (EDA)(englisch: Ethylenediamine = EDA) zeigte ein größeres
Lösungsvermögen für GeS3, so daß mit EDA weiter
experimentiert wurde. Es wurden Lösungen verschiedener
Konzentrationen von GeS3 in EDA angesetzt. Dazu wurde eine
bestimmte Mengen GeS3 in einige ml EDA eingebracht und bis
zum Sieden ( 116.5oC ) erhitzt. Die so entstehende
kräftig grüne, durchscheinende Lösung wurde dann bei 10000
min-1 für 5 Minuten bei 20oC zentrifugiert, um
Feststoffe abzuscheiden. Als Substrate für den nachfolgenden
Beschichtungsprozeß dienten Glasplättchen (sog.
Haematozytometer-(HCM)-Gläser) der
Größe 24 * 24 mm2. Diese Plättchen wurden im Reinraum der
Klasse 100/footnote[3]{d.h. 100 Teilchen pro m3}, in einer
Laborbelackungsanlage Modell 1001 S der Fa. Convac beschichtet.
Dazu wird:
Die Rotationsgeschwindigkeit wurde zwischen 500 und 6000 min-1 variiert.
Die Ansatzkonzentrationen vom GeS3 in EDA betrugen 3 - 15 %. Die
so hergestellten Schichten zeigten eine Variation der Schichtdicke von 370 - 47 nm
und konnten bei gleicher Legierung und zügiger Verarbeitung
reproduziert werden. Die
GeSx:EDA-Lösung war nicht lange stabil. Nach einem Tag Lagerung bei
Zimmertemperatur entfärbte sich die Lösung, und eine milchig graue Trübung
hatte sich gebildet. Durch Auswägung dünner GeSx-beschichteter
HCM-Deckgläser auf einer Mikrowaage der Fa. Cahn und
anschließender Dickenbestimmung mittels Talystep-Profilometer der
Fa. Talystep-Hobson konnte die Dichte der bei 200oC
für 30 Minuten gebackenen Schichten bestimmt werden (siehe Tabelle).
Ansatzkonzentration [Gew.%] Schichtdichte [g/cm3] 7.8 3.1(2) 11.2 2.6(2) 12.6 2.7(4) 15 2.3(2)
Mittels Atom-Absorptions-Spektroskopie (siehe den Abschnitt) konnte
der Germaniumgehalt und damit das x in der Formel
GeSx bestimmt werden. Das x zeigt eine starke Abhängigkeit
von der Ausbacktemperatur und -dauer (siehe Tabelle).
Das Ausbacken fand in diesem Falle im nicht evakuiertem Ofen
statt. Der x-Wert fällt mit wachsender Ausheiztemperatur und
-dauer.
Ansatzkonz. [Gew.%] Ausbacktemperatur [ oC ] Ausbackdauer [h] X-Wert 10 200 1 5.4(2) 10 200 2 4.8(1) 10 200 3 4.1(2) 10 200 4 4.0(2) 10 150 1 8.3(2) 10 150 2 7.8(4) 10 150 18 6.2(1) 10 150 20 6.1(1) 10 150 24 6.5(1) 15 200 1 4.7(2) 15 200 2 4.2(1)
Voraussetzung für diese x-Wert-Bestimmung ist, daß das Lösungsmittel nach einer Stunde des Ausheizens verdampft ist. In der Schicht nach dem Ausheizen verbleibendes EDA vergrößert die Schichtmasse. Da der Germaniumgehalt gemessen wird, täuscht dies einen hohen S-Anteil vor. Der Versuch, die so gewonnenen GeSx-Schichten lithographisch zu nutzen, scheiterte. Die Sensibilisierung (siehe wetsens), d.h. die Bildung einer silberhaltigen Schicht, fand zwar statt, nach der Belichtung konnte auch ein latentes Bild festgestellt werden, dies konnte aber nicht entwickelt werden. Bei der Belackung im Reinraum mit der GeSx:EDA-Lösung bildete sich ein gelblicher, pulvriger Niederschlag innerhalb der Schleuderapparatur. Dabei handelt es sich vermutlich um vom EDA-Dampf verschleppten Schwefel, der sich an kühlen Teilen absetzte. Diese Kontamination und der Mißerfolg bei der Lithographie führten zur Einstellung der Schleuderversuche. Diese Untersuchungen wurden trotzdem so ausführlich geschildert, weil dies Verfahren eine Möglichkeit aufzeigt, z.B. GeSx-Sputtertargets mit hohem x herzustellen. Solche Sputtertargets könnten in einer Sputteranlage dazu dienen, dünne schwefelreiche GeSx-Schichten herzustellen.
Die Absorption von Energie durch Gasatome im Grundzustand ist die Basis der Atom-Absorptions-Spektroskopie (AAS). Freie Atome im Grundzustand lassen sich am einfachsten durch Verdampfung erzeugen. Dazu wird die zu untersuchende Probe in Lösung gebracht und in einer geeigneten Brennerflamme unter definierten Bedingungen bzgl. Temperatur und Ausmaße, injiziert. In der Flamme wird das Lösungsmittel ausgetrieben, die Moleküle dissoziert und ein Gas freier Atome erzeugt. Der größte Teil der Atome befindet sich im Grundzustand, doch kommen auch Ionen, Elektronen und angeregte Atome vor. Die Lebensdauer des angeregten Zustandes ist in der Größenordnung von 10-9 bis 10-10 Sekunden. Wird durch diese Brennerflamme Licht der Anregungsenergie der Atome geschickt, tritt Absorption ein. Als Anregungslichtquelle werden spezielle Spektrallampen, die Hohlkathodenlampen, benutzt. Dabei handelt es sich um gleichstrombetriebene Gasentladungsröhren. Die Kathoden bestehen aus dem anzuregenden Material und haben eine Becherform. Beim Röhrengas handelt es sich zumeist um Argon oder Neon bei einem Druck von einigen hPa. Durch Anlegen einer Spannung zwischen der Anode und der Kathode wird das Edelgasplasma gezündet. Beim Bombardement des Kathodenmaterials mit den Edelgasionen werden Kathodenmaterialatome herausgeschlagen und angeregt, teilweise auch ionosiert. Bei der Relaxation wird die elementcharakteristische Strahlung emittiert. Diese Strahlung durchsetzt die Flamme der Länge l, in die die Probenlösung injiziert wird. Nach dem Durchtritt durch die Brennerflamme wird die charakteristische Strahlung in einem Monochromator herausgefiltert und die Intensität gemessen. Simultan wird mittels eines Drehspiegels (Chopper) {englisch: chopper = Zerhacker} die Strahlung an der Brennerflamme vorbeigeführt und als Referenz in den Monochromator geführt. Es wird somit abwechselnd das Referenzsignal und das Probensignal gemessen. Die Absorption in der Flamme wird mit dem Beer-Lambertschen Gesetz erfaßt:
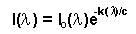 ,
,
wobei:
Durch Einführung der Extinktion als negativer dekadischer
Logarithmus der Transmission folgt:
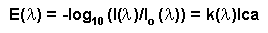
Bei meinen Untersuchungen wurde ein Atom-Absorptions-Spektrometer 4000 der Fa. Perkin-Elmer des Geochemischen Institutes der Universität Göttingen benutzt. Die Anregugswellenlänge des Germaniums beträgt lambda=265.1 nm und wurde in einer Hohlkathodenlampe erzeugt. Die Empfindlichkeit der AAS für Germanium in dieser Apparatur ist nicht sehr hoch und beträgt 2.5 µml, d.h. bei dieser Konzentration der Probenlösung tritt eine 1%ige Absorption auf. Als Brennerflamme diente ein Acethylen - Distickstoffmonoxid (Lachgas) - Gemisch, wobei das Lachgas als Oxidationsmittel gebraucht wird. Bei diesem Brenngasgemisch wird die Flamme für die Germaniumanalyse optimal, was die Dissoziation und die Grundzustandsbesetzung der Atome betrifft. Die Temperatur in der Flamme beträgt 2950oC schrenk. Als Literatur zur AAS sei hier auf schrenk und welz verwiesen.
Ein klassisches Verfahren zur Herstellung dünner, homogener Schichten in der Dünnschichttechnologie ist die thermische Verdampfung im Vakuum. Alle Materialien haben einen stark temperaturabhängigen Dampfdruck, so daß sich nahezu alle Materialien verdampfen lassen. Um zu gewährleisten, daß sich die verdampften Materialien auf der gewünschten Oberfläche niederschlagen, ist die freie Weglänge der Materialmoleküle in dem Umgebungsgas zu beachten. Um den freien Flug der abdampfenden Atome oder Atomgruppen von der Verdampferquelle zum Substrat zu ermöglichen, ist der Umgebungsdruck stark zu reduzieren. Die mittlere freie Weglänge (MFW) von Luftmolekülen bei 20oC und 1013 hPa beträgt 6.6*10-7 m. Bei einem Druck von ca. 10-4 Pa beträgt die MFW aber schon 50 cm anders. Daher sind Vakuumapparaturen für die Abscheidung von Schichten durch Verdampfung vonnöten. Zur effektiven Verdampfung ist ein Dampfdruck von ca. 1 Pa nötig anders.
Schwefel und viele Schwefelverbindungen haben schon bei niedrigen Temperaturen einen relativ hohen Dampfdruck. Werden nun Schwefel oder Schwefelverbindungen verdampft, kontaminieren diese die Vakuumapparatur. Bei derart kontaminierten Anlagen führt schon eine geringe Erwärmung zum Verdampfen des Schwefels. Dies führt zu einer Erhöhung des Restgasdruckes und zur Verunreinigung der Aufdampfschichten. (Man sagt Schwefel vergiftet Vakuumapparaturen.) Aus diesem Grunde wird die im folgenden beschriebene Vakuumanlage nur für die Verdampfung von GeSx benutzt. Die Vakuumapparatur besteht aus einem Edelstahlrezipienten mit einigen CF-Flanschen zur Aufnahme von Pumpstutzen, mechanischen Manipulatoren, elektrischen und Kühlwasser-Durchführungen. Als Hochvakuumpumpe diente eine Turbomolekularpumpe Turbovac 120 ( bzw. seit Herbst 1990 eine Turbovac 150 CSV ) samt Steuereinheit Turbotronic 120 der Fa. Leybold-Haeraus. Den Vorvakuumdruck liefert eine zweistufige Drehschieberpumpe EDM 12 der Fa. Edwards. Als Meßgeräte sind am Rezipienten folgende Amaturen angebracht:
Die Vakuummeßgeräte sind mit der Meßeinheit PKG 020 verbunden.
Die Vakuummeßgeräte sind von der Fa. Balzers. Der Schwingquarz ist
Teil des Inficon XTM Schichtdickenmonitors der Fa. Leybold-Haeraus.
Zur Stromversorgung der Verdampferquelle dient ein zweistufiger Transformator.
Zum einen ein Stelltrafo, der bei einer Eingangsspannung von 220 V eine
Ausgangsspannung von 0-220 V liefert. Zum anderen ein
Festtrafo,
der bei einer Eingangsspannung von 220 V eine Ausgangsspannung von
2*2.5 V liefert. Die maximale Betriebslast beträgt 1.5 kW, was bei
2.5 V Ausgangsspannung einem Strom von 600 A entspricht.
Die Trafos wurden von der Fa. Ruhstrat bezogen. Die elektrischen, mechanischen und
Wasser-Durchführungen wurden bei der Fa. Edwards bestellt oder in der
Institutswerkstatt hergestellt. Die Abbildung zeigt den
derzeitigen (Frühjahr 1991) Aufbau.
Aufbau der Verdampferanlage
Die Anlage arreicht nach ca. 2 Stunden ein Arbeitsvakuum von 5*10-4 Pa.
Bei der einfachen thermischen Verdampfung wird das zu verdampfende Material in ein direkt durch elektrische Widerstandsheizung erhitztes Verdampferschiffchen gebracht. Das Verdampferschiffchen besteht aus einem dünnen Metallblech aus Tantal, Molybdän oder Wolfram (siehe Abb.).
Aufbau der einfachen thermischen Verdampfung
Erste Versuche zur Verdampfung der selbst hergestellten Legierung wurden mit offenen Wolframschiffchen ausgeführt. Bei der Erhitzung des Schiffchens auf leichte Rotglut, das sind ca. 600oC , war zu beobachten, daß das Verdampfungsmaterial, das Evaporat, auf seinem eigenen Dampf schwebt. Durch diese thermisch isolierende Dampfschicht wurde die Aufdampfrate beschränkt. Teilweise wurde das Evaporat aus dem Schiffchen geschleudert. Auf den resultierenden GeSx-Schichten wurden nach der Belichtung und Entwicklung kleine tropfenförmige Verunreinigung festgestellt. Es ist anzunehmen, daß diese Tropfen aus dem Schiffchen auf das Substrat geschleudert wurden.
Mit Flash-Verdampfung wird die blitzartige Verdampfung
des Evaporates durch Aufstreuen auf ein heißes Filament oder Schiffchen
bezeichnet. Diese Verdampfung wird für die Verdampfung von Legierungen und
Verbindungen empfohlen, die zur Zersetzung bei Erhitzung neigen.
Hierbei sorgt eine kontinuierliche Zuführung des Evaporates auf den heißen
Verdampfer für eine in ihrer Zusammensetzung konstante, chemisch
homogene Schicht auf dem Substrat. Durch den heißen Verdampfer soll gewährleistet werden, daß
auch die erst bei höheren Temperaturen verdampfenden Bestandteile augenblicklich
beim Kontakt mit dem Verdampfer in die Gasphase übergehen.
Aufbau der Flash-Verdampfung
Zu Versuchen zur Flash-Verdampfung wurde eine kleine ca. 5 cm lange Rutsche aus Tantalblech in die Apparatur installiert (siehe Abb.). Das untere Ende des Tantalbleches befand sich ca. 1 cm über dem Verdampfer. Als Verdampfer diente ebenfalls ein dünnes Tantalblech, das direkt elektrisch bis zur Weißglut beheizt wurde. Das pulverisierte GeSx-Evaporat wurde auf die Rutsche aufgestreut. Danach wurde evakuiert und der Verdampfer hochgeheizt. Über eine mechanische Durchführung wurde die Rutsche angestoßen und in Schwingung versetzt. Das Evaporat glitt so die Rutsche herab und fiel auf den heißen Verdampfer. Beim Kontakt mit dem Verdampfer überhitzte sich das Evaporat spontan und wurde durch seinen eigenen Dampfdruck in den Rezipienten geschleudert. Der größte Teil des Evaporates ging so verloren, ohne in die Dampfphase überzugehen. Die Effizienz der Verdampfung war somit gering. Weder ein Ersatz des Verdampferbleches durch ein Schiffchen, um die Aufenthaltsdauer des Evaporates auf dem Verdampfer zu erhöhen, noch die Verringerung der Verdampfertemperatur führten zum Erfolg. Die hierbei hergestellten Schichten ließen sich lithographisch nutzen, zeigten aber tropfenförmige Flecken nach der Entwicklung.
Als Effusionszellen werden Verdampferschiffchen bezeichnet, bei
denen das Evaporat im Schiffchen eingesperrt ist. Der beim Erhitzen entstehende
Dampf des Evaporates muß seinen Weg in den Rezipienten durch ein Labyrinth
aus heißen Blechen und Sieben nehmen. Diese Verdampfer bieten den Vorteil, daß
das Evaporat im engen Kontakt mit dem Verdampfer steht und keine Teilchen
herausgeschleudert werden können. Diese Verdampfer lassen eine gute Effizienz
bzgl. der Qualität der aufgedampften Schichten und der Ausbeute des
Evaporates erwarten.
Knudtsenzellen stellen die Idealform der Effusionszellen dar. Bei diesen ist
die Größe der Öffnung des Verdampfers ca. 1/10 der mittleren
freien Weglänge (MFW) der Dampfmoleküle im Verdampfer. Die Oberfläche
des Evaporates in der Knudtsenzelle ist sehr viel größer als die Öffnung.
In der Zelle kann sich somit ein quasi thermischer Gleichgewichtsdampfdruck
aufbauen. Nur ein sehr dünner Molekülstrom kann die Zelle verlassen, die
Aufdampfraten sind gering handbook.
Zu diesen Untersuchungen wurden kommerzielle Molybdänschiffchen des Typs:
BD 482 061-T der Fa. Balzers verwendet. Diese bestehen aus 0.1 mm starkem
Molybdänblech mit einem Fassungsvermögen von 5 cm3 Evaporat (siehe
Abb.).

Aufbau der Effusionszellenverdampfung
Innen ist ein Siebblech angebracht und die Austrittsöffnung hat einen
Durchmesser von 5 mm. Das gesamte Schiffchen ist stromdurchflossen,
so daß alle Teile heiß werden. Um eine Temperatur von 1400oC zu
erreichen, muß
ein Heizstrom von 290 A eingestellt werden, die Leistungsaufnahme beträgt
dann 420 W [lt. Katalog]. Die Stromversorgung erfolgte durch eine wassergekühlte
Hochstrom-Vakuumdurchführung der Fa. Edwards und einen wassergekühlten Massesockel,
der in der Institutswerkstatt gefertigt wurde.
Bei der Verdampfung der selbst hergestellten Legierung kam es trotz allem zum
Auswurf von Evaporat, der sich aber auf den Schichten nicht bemerkbar machte. Die
Schichten waren auch nach der Entwicklung homogen. Mit dieser
Verdampferquelle wurden quantitativ analytische Verdampfungen
angestellt, um die Zusammensetzung der Schichten im Verlauf der
Verdampfung zu bestimmen.
Das Evaporat wurde in das Schiffchen eingewogen. Ca. 8 cm oberhalb
der Verdampferöffnung wurden je Verdampfung zwei mit der Cahn-Mikrowaage ausgewogene
HCM-Deckgläser angebracht (siehe Abb.). Diese wurden solange bedampft, bis die Schichtdicke
am Ort des Substrathalters ca. 100 nm betrug. Die Gläser wurden dann gegen
neue ausgetauscht und die Verdampfung wiederholt. Dies wurde bis zur vollständigen
Entleerung des Schiffchens fortgesetzt. Die abgeschiedene GeSx-Menge
wurde ausgewogen und in eine abgemessene Menge 2 %iger KOH-Lösung
gebracht, um
das Kondensat zu lösen. Der Germaniumgehalt dieser Lösung wurde mittels
Atom-Absorptions-Spektroskopie (AAS) bestimmt. Da die Germanium-Standard-Lösungen für die AAS eine KOH-Konzentration von 2 %
aufwiesen,
war es nötig, diese Konzentration auch für die zu untersuchenden Lösungen
zu verwenden. Es zeigte sich aber, daß GeSx-Schichten mit x > 7
sich nicht in 2 %iger KOH lösen. Die ersten
kondensierten Schichten
der Verdampfung ließen sich daher nicht analysieren (siehe
Abb.).
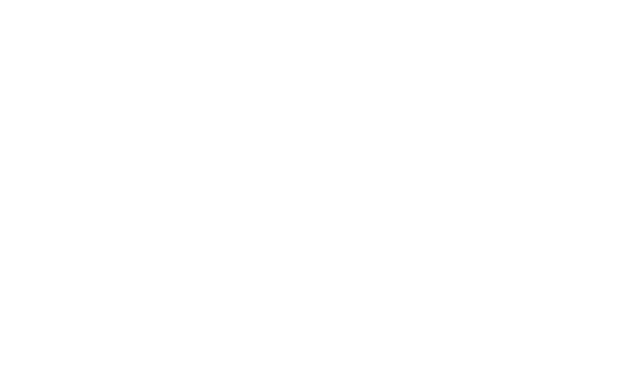
Disproportionierung von GeSx aus eigener Legierung bei der Verdampfung aus einer Effusionszelle
Aus den Analysen folgte, daß sich nach der Niederschlagung von 1 µm am Ort des Substrathalters aus einer Einwaage von 2.2 g der GeS3-Legierung bzw. von 0.8 µm von 2 g der GeS2-Legierung eine dann nahezu konstant bleibende Schichtzusammensetzung von GeS1.2 einstellt.
Bei einem Forschungsaufenthalt im Rahmen eines von der DFG geförderten
Austausches mit der Bulgarischen Akademie der Wissenschaften im Zentrallabor
für Photographische Prozesse in Sofia lernte ich die 3-Quellen-Verdampfungsanlage
von Asparuch Panov kennen. Zur Herstellung der Germaniumsulfidschichten
werden eine Germanium- und eine Schwefel-Verdampfungsquelle angesteuert.
Die einzelnen Quellen werden separat beheizt und eingestellt, bis sie
stabile gewünschte
Aufdampfraten zeigen. Danach werden durch das simultane Aufdampfen von
Germanium und Schwefel die GeSx-Schichten direkt auf den Substraten erzeugt.
Anschließend wird wie zuvor nur mit der Schwefel- und einer Silberquelle
eine trockene Sensibilisierung mit Ag2S durchgeführt. In Sofia konnten
Belichtungsversuche mit so hergestellten GeS2:Ag2S-Schichten gemacht
werden.
Nach den in Sofia gemachten Erfahrungen wurden Versuche
unternommen, eine 3-Quellenverdampfung in der hiesigen Anlage zu
installieren. Es wurden 3 Stromdurchführungen installiert. Besonderer
Wert mußte darauf gelegt werden, daß die Schwefelquelle thermisch von
den anderen Quellen isoliert ist.
Als Silberquelle diente ein einfaches offenes Molydänschiffchen. Als
Germaniumquelle diente ein dickeres Wolframschiffchen. Das dickere
Wolframschiffchen mußte gewählt werden, da zum einen ein größeres
Reservoir an Germanium für die Stabilität der Quelle gebraucht wurde und
zum anderen Germanium mit dem heißen Wolframschiffchen legiert und
dieses zerstört.
Als Schwefelquelle diente die schon in beschriebene Effusionsquelle.
Diese wurde in einen ausgehöhlten, wassergekühlten Aluminiumklotz
gespannt, um die Wärmebelastung durch die Emission der anderen Quellen zu
reduzieren.
Die Temperatur der Germanium- und der Silberquelle wurde nicht
gemessen. Die Temperatur der Schwefelquelle wurde mit einem Thermoelement gemessen.
In den Abbildungen sind typische Verdampfungskurven der
Germanium- und der
Silberquelle gezeigt. Beim Germanium fällt der sprunghafte Anstieg
der Aufdampfrate nach 2500 Sekunden ins Auge. Die Quelle wurde mit einer
konstanten Spannung über die ganze Zeit betrieben. Nach der Verdampfung
war die Quelle aufgrund der legierungsbedingten Versprödung nicht mehr zu
gebrauchen. Der Sprung in der Kurve wird auf die Legierung des
Germaniums mit dem Wolfram und der damit einhergehenden Widerstandsänderung
des Schiffchens zurückzuführen sein. Beim Silberschiffchen bricht die stabile
Verdampfung nach 1500 Sekunden ab, was seinen Grund in der
Erschöpfung des Silberreservoirs hat. Die Temperatur bleibt zwar
konstant, aber
die dampfende Oberfläche wird kleiner und die Aufdampfrate sinkt.
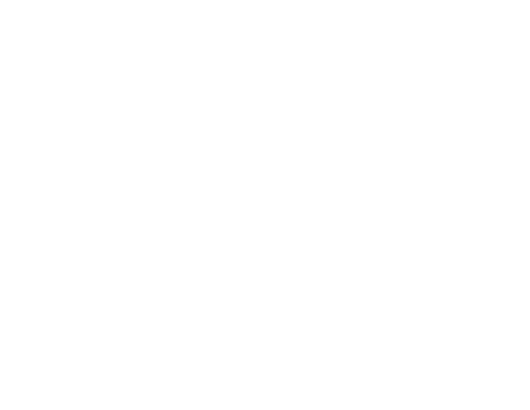
Zeitliche Stabilität der Germaniumverdampfung bei der einfachen thermischen Verdampfung: Aufdampfrate und Schichtdicke gegen die Aufdampfzeit
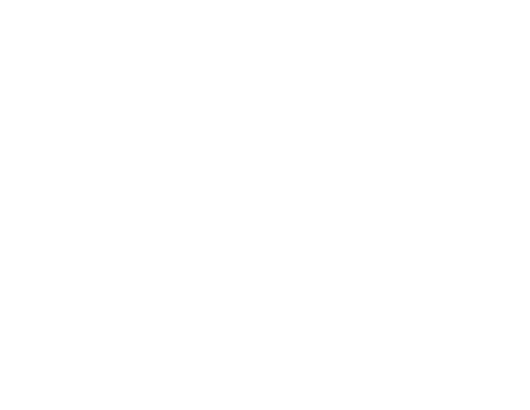
Zeitliche Stabilität der Silberverdampfung bei der einfachen thermischen Verdampfung: Aufdampfrate und Schichtdicke gegen die Aufdampfzeit
Bei der Schwefelquelle gab es Probleme, die in dieser Apparatur nicht beseitigt
werden konnten. Beim alleinigen Betrieb der Schwefelquelle schied
sich ein großer Teil des verdampfenden Schwefels am Rand des
Aluminiumklotzes
ab. Die ungekühlten Substrate verdampften ebensoviel Schwefel wie
auf ihnen kondensierte, so daß kein Schichtwachstum auf den
Substraten festgestellt werden konnte. Auf dem Schgwingquarz
konnte aufgrund der ständigen Wasserkühlung des Quarzes eine
Schwefelabscheidung gemessen werden. Als größtes Problem der
stabilen Schwefelverdampfung erwieß sich aber die Wärmelast durch
die in Betrieb befindliche Germaniumquelle. Der Wärmefluß über
den gemeinsamen Massesockel war so groß, daß keine kontrollierte
Verdampfung aus der Schwefelquelle möglich war. Da eine Trennung
der Massesockel aufgrund des Platzmangels im Rezipienten und der
Neuaufbau einer Mehrquellenverdampfungsanlage aus Zeitmangel nicht
möglich waren, wurden diese Versuche eingestellt.
Die Effusionszellenverdampfung stellte sich im Rahmen dieser Arbeit
als die beste Methode zur Herstellung reproduzierbarer
Chalkogenidschichten heraus. Die Schichten waren homogen und von
kontrollierbarer Zusammensetzung. Daher wurden in den folgenden
Untersuchungen, wenn nichts anderes erwähnt wird,
Germaniumsulfidschichten verwendet, die mittels
Effusionszellenverdampfung aufgebracht worden sind.